Чему равна энергия поверхностного слоя жидкости. Поверхностный слой жидкости
Почти все физические и химические процессы в природе связаны с взаимодействием между атомами. Величиной межатомных сил определяются физико-химические свойства газообразных, жидких и твердых веществ. Процессы смачивания и капиллярного течения жидкостей по поверхности твердого или жидкого тела также обусловлены наличием в них внутренних и поверхностных силовых полей. Проявление этих сил вызывает взаимодействия между молекулами внутри и на поверхности жидкости. Изолированная молекула, находящаяся внутри жидкости на расстоянии радиуса действия молекулярных сил, притягивает окружающие молекулы и одновременно находится под воздействием этих молекул. Равнодействующая всех сил равна нулю, в результате молекула внутри жидкости находится в равновесии. При перемещении молекулы к поверхности на расстояние, меньшее радиуса действия молекулярных сил, условие ее равновесия будет другим.
Молекулы жидкости, находящиеся на поверхности ее раздела с газом, испытывают значительно большее притяжение со стороны жидкости, чем со стороны газовой среды, отличающейся малой плотностью. Вследствие этого возникает направленная внутрь жидкости сила, стремящаяся переместить ее молекулы с поверхности в глубину. Поверхность жидкости ведет себя подобно туго натянутой резиновой пленке. Образуется поверхностный слой, который оказывает давление на жидкость. Толщина этого слоя составляет приблизительно 10 А. Энергия молекул вблизи поверхности раздела выше, чем внутри жидкости. Свободная энергия поверхностного слоя направлена во всех точках перпендикулярно к поверхности и стремится сократить ее до минимума. Если другие силы не действуют на жидкость, она принимает форму шара, т.е. тела с наименьшей поверхностью при данном объеме.
При решении практических задач сложно оперировать с поверхностной энергией жидкости, поэтому введено более простое понятие о коэффициенте поверхностного натяжения s, численно равном силе поверхностного натяжения, приходящейся на единицу длины ПС жидкости и действующей в направлении, перпендикулярном к этой линии
s = F / L (5.1)
где F - сила поверхностного натяжения, Н; L - длина свободной поверхности жидкости, на которой действует сила поверхностного натяжения F, м.
Неравноценность молекулярного взаимодействия на границе раздела фаз и втягивания поверхностных молекул внутрь жидкости вызывают появление силы. Эта сила действует тангенциально, рассчитывается на единицу длины периметра, ограничивающего поверхность жидкости, и называется поверхностным натяжением.
Поскольку поверхностное натяжение действует тангенциально к поверхности жидкости, ее поверхностный слой (ПС) всегда будет ровный и гладкий, на нем отсутствуют выступы. Поверхностное натяжение имеет размерность Н/м или дин/см. Для воды оно равно при 20°С 72,75*10 -3 Н/м, или 72,75 мН/м (миллиньютон на метр).
Нескомпенсированность молекулярного взаимодействия, стремление молекул ПС втягиваться во внутрь жидкости, а также вызванное этим поверхностное натяжение жидкости на границе с другой жидкостью (s жж) или с газовой средой (s жг), стремятся сократить поверхность жидкости до минимальных размеров. Наименьшей поверхностью при данном объеме обладает сфера. Сферическую поверхность можно наблюдать у относительно малых капель некоторых жидкостей, например, ртути, на стекле, покрытом парафином. Это явление используется для получения сферических частиц металлических порошков путем распыления жидкого металла. Для того, чтобы увеличить поверхность жидкости, то из ее объема следует вытягивать на поверхность новые частицы, т.е. совершать работу против сил, которые заставляют поверхность жидкости уподобляться пленке и носят название сил поверхностного натяжения. Из этого следует, что уменьшение поверхности жидкости должно сопровождаться и уменьшением свободной энергии, т.е. оно является самопроизвольным процессом. Этим объясняется то, что свободная взвешенная в воздухе жидкость стремится принять форму шарообразных капель, т.к. шар при заданном объеме имеет наименьшую величину поверхности. По этой же причине мелкие капли жидкости при соприкосновении сливаются в более крупные - при одинаковом объеме поверхность крупной капли меньше, чем нескольких мелких. Значение поверхностной энергии жидкости и изменение под действием ее формы капли зависит от природы взаимодействующих веществ, соприкасающихся на границе раздела фаз. Чем ближе по величине значения их поверхностной энергии, тем меньше результирующая межфазная поверхностная энергия.
Поверхностное натяжение может проявляться как сила.
Как видно, величину s жг можно рассматривать как энергию, отнесенную к единице поверхности (площади), и как силу, отнесенную к единице длины периметра поверхности. С точки зрения размерностей это одно и то же. Действительно,
s = E / S = m l 2 t -2 / l 2 = m l t -2 / l = F / l (5.2)
Здесь E - энергия; S - площадь; m - размерность массы; l - размерность длины; t - размерность времени.
Таким образом, размерность удельной свободной поверхностной энергии - Дж/м 2 , а размерность поверхностного натяжения - Н/м. Для однокомпонентной жидкости, например воды, численные значения поверхностного натяжения и удельной свободной поверхностной энергии равны между собой. У жидкостей, в состав которых входит несколько веществ, подобное совпадение отсутствует. Различие между поверхностным натяжением и удельной свободной поверхностной энергией незначительно, и в большинстве случаев эти понятия отождествляют. Иногда для подчеркивания энергетического аспекта в образовании новой поверхности размерность поверхностного натяжения дают в мДж/м 2 .
Необходимо заметить, что удельная свободная поверхностная энергия не является особой формой энергии, а представляет тот избыток энергии в расчете на единицу поверхности, которым обладают молекулы на поверхности в связи с их положением. Помимо удельной различают свободную поверхностную энергию. Если термин "удельная" относится к единице площади поверхности, то термин "свободная" - ко всей поверхности. При этом слово "поверхностная" обычно опускают, подразумевая, что свободная энергия относится к поверхности раздела фаз.
Поверхностное натяжение можно также выразить как работу, которую необходимо затратить, чтобы увеличить поверхность жидкости на 1 единицу поверхности. Величина поверхностного натяжения жидкости зависит от природы среды, с которой она граничит. Поверхностное натяжение часто относят к границе с воздухом и обозначают s.
Поверхностное натяжение является вектором, модуль которого имеет размерность Н/м. Поверхностная же энергия является величиной скалярной и выражает работу, необходимую для образования новой поверхности. В отношении жидкости понятия поверхностного натяжения и поверхностной энергии в количественном смысле равны.
Поверхностное натяжение, или, в общем случае, межфазное натяжение обусловлено тем, что частицы жидкости испытывают преимущественное притяжение одной из фаз. В рассмотренном взаимодействии молекул основное влияние на ПС оказывает сама жидкость, в то время как вторая фаза, в данном случае газовая атмосфера, оказывает на ПС незначительное влияние. Чем резче выражена эта ассиметрия силовых полей, тем больше величина поверхностного натяжения. В тех случаях, когда различие в силовых полях проявляется в меньшей степени, поверхностное натяжение имеет низкие значения. В растворах частицы с сильными силовыми полями вытесняют на поверхность частицы с более слабыми силовыми полями. Повышение концентрации их в ПС вызывает снижение поверхностного натяжения. Если отдельные компоненты взаимодействующих систем, например, легирующие элементы в сплавах, имеют силовое поле, близкое по значению силовому полю основы сплава, то эти компоненты практически распределены равномерно и представляют собой растворы, свойства которых близки к идеальным.
Для однокомпонентных систем коэффициент поверхностного натяжения на границе твердое тело - вакуум имеет максимальное значение, на границе жидкость - насыщенный пар - более низкое значение, на границе твердое тело - жидкость коэффициент поверхностного натяжения имеет наименьшее значение.
Растекание жидкости и смачивание ими поверхности твердого тела сопровождается увеличением поверхности, связанным с преодолением сил поверхностного натяжения.
Интенсивность процесса смачивания поверхности металлов приблизительно можно оценить количеством выделяемой при этом энергии.
Смачивание оказывает существенное влияние на процессы сцепления между двумя металлами, один из которых находится в твердой, а другой в жидкой фазе. Это является отличительным признаком пайки, однако и в условиях сварки оказывает большое влияние на качество сварных соединений. Так, от смачиваемости металла расплавом зависит форма шва, а, следовательно, и вибропрочность сварных соединений. Нежелательным явлением служит сцепление жидких капель с основным металлом - налипание брызг. Это явление особенно часто наблюдается при сварке в углекислом газе, порошковой проволокой без флюса, при ручной дуговой сварке. Решающую роль играет сцепление между жидким расплавом и твердым металлом в процессах, занимающих промежуточное положение между сваркой и пайкой - омеднении, алитировании и др. Необходимым условием установления металлической связи между атомами твердого и жидкого металла является сближение атомов, которое достигается при смачивании твердого тела жидким. С энергетической точки зрения самопроизвольно такое смачивание будет происходить только в том случае, если работа сил притяжения между жидкостью и твердым металлом (работа адгезии) будет равна или больше работы сил притяжения частиц жидкости друг к другу (работа когезии).
Смачивание зависит от химического сродства между контактирующими металлами, и в первую очередь, от их взаимной растворимости. Металлы, образующие взаимные растворы или химические соединения и имеющие общие фазы на диаграмме состояний, обычно обладают хорошей взаимной смачиваемостью. Как правило, металлы хорошо смачиваются собственным расплавом. Нерастворимые друг в друге металлы чаще всего обладают плохой взаимной смачиваемостью (Fe - Pb, Al - Pb, Cu - Pb). Смачивание улучшается также при меньшей разнице температур плавления.
Знаете ли Вы, в чем ложность понятия "физический вакуум"?
Физический вакуум - понятие релятивистской квантовой физики, под ним там понимают низшее (основное) энергетическое состояние квантованного поля, обладающее нулевыми импульсом, моментом импульса и другими квантовыми числами. Физическим вакуумом релятивистские теоретики называют полностью лишённое вещества пространство, заполненное неизмеряемым, а значит, лишь воображаемым полем. Такое состояние по мнению релятивистов не является абсолютной пустотой, но пространством, заполненным некими фантомными (виртуальными) частицами. Релятивистская квантовая теория поля утверждает, что, в согласии с принципом неопределённости Гейзенберга, в физическом вакууме постоянно рождаются и исчезают виртуальные, то есть кажущиеся (кому кажущиеся?), частицы: происходят так называемые нулевые колебания полей. Виртуальные частицы физического вакуума, а следовательно, он сам, по определению не имеют системы отсчета, так как в противном случае нарушался бы принцип относительности Эйнштейна, на котором основывается теория относительности (то есть стала бы возможной абсолютная система измерения с отсчетом от частиц физического вакуума, что в свою очередь однозначно опровергло бы принцип относительности, на котором постороена СТО). Таким образом, физический вакуум и его частицы не есть элементы физического мира, но лишь элементы теории относительности, которые существуют не в реальном мире, но лишь в релятивистских формулах, нарушая при этом принцип причинности (возникают и исчезают беспричинно), принцип объективности (виртуальные частицы можно считать в зависимсоти от желания теоретика либо существующими, либо не существующими), принцип фактической измеримости (не наблюдаемы, не имеют своей ИСО).
Когда тот или иной физик использует понятие "физический вакуум", он либо не понимает абсурдности этого термина, либо лукавит, являясь скрытым или явным приверженцем релятивистской идеологии.
Понять абсурдность этого понятия легче всего обратившись к истокам его возникновения. Рождено оно было Полем Дираком в 1930-х, когда стало ясно, что отрицание эфира в чистом виде, как это делал великий математик, но посредственный физик , уже нельзя. Слишком много фактов противоречит этому.
Для защиты релятивизма Поль Дирак ввел афизическое и алогичное понятие отрицательной энергии, а затем и существование "моря" двух компенсирующих друг друга энергий в вакууме - положительной и отрицательной, а также "моря" компенсирующих друг друга частиц - виртуальных (то есть кажущихся) электронов и позитронов в вакууме.
Наиболее характерным свойством жидкости, отличающим ее от газа, является то, что на границе с газом жидкость образует свободную поверхность, наличие которой приводит к возникновению явлений особого рода, называемых поверхностными. Своим возникновением они обязаны особым физическим условиям, в которых находятся молекулы вблизи свободной поверхности.
На каждую молекулу жидкости действуют силы притяжения со стороны окружающих ее молекул, расположенных от нее на расстоянии порядка м (радиус молекулярного действия). На молекулу , расположенную внутри жидкости (рис. 1), действуют силы со стороны таких же молекул, и равнодействующая этих сил близка к нулю.

Для молекул равнодействующие сил отличны от нуля и направлены внутрь жидкости, перпендикулярно к ее поверхности. Таким образом, все молекулы жидкости, находящиеся в поверхностном слое, втягиваются внутрь жидкости. Но пространство внутри жидкости занято другими молекулами, поэтому поверхностный слой создает давление на жидкость (молекулярное давление ).
Чтобы переместить молекулу , расположенную непосредственно под поверхностным слоем, на поверхность, необходимо совершить работу против сил молекулярного давления. Следовательно, молекулы поверхностного слоя жидкости обладают дополнительной потенциальной энергией по сравнению с молекулами внутри жидкости. Эту энергию называют поверхностной энергией .
Очевидно, что величина поверхностной энергии тем больше, чем больше площадь свободной поверхности.
Пусть площадь свободной поверхности изменилась на , при этом поверхностная энергия изменилась на ![]() , где a - коэффициент поверхностного натяжения.
, где a - коэффициент поверхностного натяжения.
Так как для этого изменения необходимо совершить работу
Единицей коэффициента поверхностного натяжения в СИ является джоуль на квадратный метр .
Коэффициент поверхностного натяжения - величина, численно равная работе, совершенной молекулярными силами при изменении площади свободной поверхности жидкости на единицу при изотермическом процессе.
Так как любая система, предоставленная сама себе, стремится занять такое положение, в котором ее потенциальная энергия наименьшая, то жидкость обнаруживает стремление к сокращению свободной поверхности.
Поверхностный слой жидкости ведет себя подобно растянутой резиновой пленке, т.е. все время стремится сократить площадь своей поверхности до минимальных размеров, возможных при данном объеме.
Пример: капля жидкости в состоянии невесомости имеет сферическую форму.
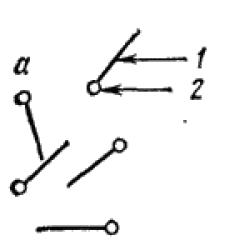
На поверхности жидкости, вблизи границы, разделяющей жидкость и ее пар, взаимодействие между молекулами жидкости отличается от взаимодействия молекул внутри объема жидкости. Для иллюстрации этого утверждения рассмотрим рис. 20 . Молекула 1, окруженная со всех сторон другими молекулами той же жидкости испытывает в среднем одинаковые силы притяжения ко всем своим соседям. Равнодействующая этих сил близка к нулю. Молекула 2 испытывает меньшее притяжение вверх со стороны молекул пара и большее притяжение вниз со стороны молекул жидкости. В результате на молекулы, расположенные в поверхностном слое действует направленная вниз в глубь жидкости равнодействующая R сил, которую принято относить к единице площади поверхностного слоя.
Для перенесения молекул из глубины жидкости в ее поверхностный слой необходимо совершить работу по преодолению силы R . Эта работа идет на увеличение поверхностной энергии , т.е. избыточной потенциальной энергии, которой обладают молекулы в поверхностном слое по сравнению с их потенциальной энергией внутри остального объема жидкости.
Обозначим потенциальную энергию одной молекулы в поверхностном слое, - потенциальную энергию молекулы в объеме жидкости, – число молекул в поверхностном слое жидкости. Тогда поверхностная энергия равна
![]()
Коэффициентом поверхностного натяжения (или просто поверхностным натяжением ) жидкости называют изменение поверхностной энергии при изотермическом увеличении площади поверхности на одну единицу:
![]() ,
,
где – число молекул на единице площади поверхности жидкости.
Если поверхность жидкости ограничена периметром смачивания (см. 4.3), то коэффициент поверхностного натяжения численно равен силе, действующей на единицу длины периметра смачивания и направленной перпендикулярно к этому периметру:
где – длина периметра смачивания, – сила поверхностного натяжения, действующая на длине периметра смачивания. Сила поверхностного натяжения лежит в плоскости, касательной к поверхности жидкости.
Сокращение площади поверхности жидкости уменьшает поверхностную энергию. Условием устойчивого равновесия жидкости, как и любого тела, является минимум потенциальной поверхностной энергии. Это значит, что в отсутствие внешних сил жидкость должна иметь при заданном объеме наименьшую площадь поверхности. Такой поверхностью является сферическая поверхность.
Для уменьшения поверхностного натяжения жидкости к ней добавляют специальные примеси (поверхностно-активные вещества), которые располагаются на поверхности и уменьшают поверхностную энергию. К ним относятся мыло и другие моющие средства, жирные кислоты и т.п.
Смачивание и несмачивание
На границе соприкосновения жидкостей с твердыми телами наблюдаются явления смачивания , состоящие в искривлении свободной поверхности жидкости около твердой стенки сосуда. Поверхность жидкости, искривленная на границе с твердым телом, называется мениском. Линия, по которой мениск пересекается с твердым телом, называется периметром смачивания.

 Явление смачивания характеризуется краевым углом
q между поверхностью твердого тела и мениском в точках их пересечения, т.е. в точках периметра смачивания. Жидкость называется смачивающей
твердое тело, если краевой угол острый 0£q
Явление смачивания характеризуется краевым углом
q между поверхностью твердого тела и мениском в точках их пересечения, т.е. в точках периметра смачивания. Жидкость называется смачивающей
твердое тело, если краевой угол острый 0£q
Различие краевых углов в явлениях смачивания и несмачивания объясняется соотношением сил притяжения между молекулами твердых тел и жидкостей и сил межмолекулярного притяжения в жидкостях. Если силы притяжения между молекулами твердого тела и жидкости больше, чем силы притяжения молекул жидкости друг к другу, то жидкость будет смачивающей. Если молекулярное притяжение в жидкости превышает силы притяжения молекул жидкости к молекулам твердого тела, то жидкость не смачивает твердое тело.
Искривление поверхности жидкости создает дополнительное (избыточное) давление на жидкость по сравнению с давлением под плоской поверхностью (Лапласово давление). Для сферической поверхности жидкости это давление выражается формулой:
![]() ,
,

 где s - коэффициент поверхностного натяжения, – радиус сферической поверхности; > 0, если мениск выпуклый; < 0, если мениск вогнутый (рис. 23). При выпуклом мениске увеличивает то давление, которое существует под плоской поверхностью жидкости (например, атмосферное давление на свободную поверхность жидкости). При вогнутом мениске давление под плоской поверхностью уменьшается на величину (рис. 24). Дополнительное давление внутри сферического пузыря радиуса R вызывается избыточным давлением на обеих поверхностях пузыря и равно = 4s ¤ R
.
где s - коэффициент поверхностного натяжения, – радиус сферической поверхности; > 0, если мениск выпуклый; < 0, если мениск вогнутый (рис. 23). При выпуклом мениске увеличивает то давление, которое существует под плоской поверхностью жидкости (например, атмосферное давление на свободную поверхность жидкости). При вогнутом мениске давление под плоской поверхностью уменьшается на величину (рис. 24). Дополнительное давление внутри сферического пузыря радиуса R вызывается избыточным давлением на обеих поверхностях пузыря и равно = 4s ¤ R
.
Капиллярные явления
Узкие цилиндрические трубки малого диаметра (< 1 мм) называются капиллярами .
Если опустить такой капилляр в несмачивающую жидкость, то под действием Лапласова давления ее уровень в капилляре понизится по сравнению с уровнем в сообщающемся с ним широком сосуде (рис. 25).

 Если капилляр опустить в смачивающую жидкость, то ее уровень в капилляре по той же причине повысится (рис. 26). В случае идеального смачивания , а при идеальном несмачивании . Тогда из условия равновесия жидкости можно найти высоту подъема (или опускания) жидкости в капилляре:
Если капилляр опустить в смачивающую жидкость, то ее уровень в капилляре по той же причине повысится (рис. 26). В случае идеального смачивания , а при идеальном несмачивании . Тогда из условия равновесия жидкости можно найти высоту подъема (или опускания) жидкости в капилляре:
Здесь - плотность жидкости, – ускорение силы тяжести, – радиус капилляра. Изменения высоты уровня жидкости в капиллярах называются капиллярными явлениями. Этими явлениями объясняется гигроскопичность, т.е. способность впитывать влагу, ряда тел (вата, ткани, почвы, бетон).
Литература
1. Трофимова Т.И. Курс физики. - М.: Высш. школа, 2001.
2. Савельев И.В. Курс общей физики. Механика. Молекулярная физика.
– СПб.: Лань, 2006.
3. Сивухин Д.В. Общий курс физики. Молекулярная физика и термодинамика. - М.: Физматлит, 2005.
4. Детлаф А.А., Яворский Б.М. Курс физики. - М.: Высш. школа, 2001.
5. Федосеев В.Б. Физика: учебник. – Ростов н/Д: Феникс, 2009.
Введение. Предмет и задачи молекулярной физики и термодинамики…………………….3
1. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКАЯ ТЕОРИЯ ИДЕАЛЬНЫХ ГАЗОВ……………4
1.1. Основные положения молекулярно-кинетической теории………..4
1.2. Масса и размеры молекул. Количество вещества…………………... 5
1.3. Законы идеального газа ………………………………………………..……….7
1.4. Уравнение состояния идеального газа ……………………………….…10
1.5. Основное уравнение МКТ идеальных газов …………………….…….12
1.6. Закон Максвелла о распределении молекул по скоростям.…...15
1.7. Распределение Больцмана ……………………………………………………18
1.8. Средняя длина свободного пробега молекул. Явления переноса………………………………………………………………………………20
2. ОСНОВЫ ТЕРМОДИНАМИКИ…………………………………………………………….23
2. 1. Внутренняя энергия системы Степени свободы молекул ………….23
2. 2. Первое начало термодинамики. Удельная и молярная теплоемкости.…………………………………………………………………………….26
2.3. Работа газа по перемещению поршня. Теплоемкость при постоянных объеме и давлении ……………………………………………………..27
2.4. Применение первого начала термодинамики к изопроцессам. Адиабатный процесс. Политропный процесс …………………………………..29
2.5. Круговой процесс. Обратимые и необратимые процессы………….31
2.6. Энтропия………………………………………………………………………………….33
2.7. Второе и третье начала термодинамики……………………………………..37
2.8. Тепловые двигатели и холодильные машины..………………………….38
3. РЕАЛЬНЫЕ ГАЗЫ …………………………………………………………………………….41
3.1. Уравнение Ван-дер-Ваальса …………………………………………………….41
3.2. Внутренняя энергия реального газа………………………………………….42
4. Свойства жидкостей.……………………………………………………………………...44
4.1. Особенности жидкого состояния вещества
4.2. Энергия поверхностного слоя и поверхностное натяжение жидкостей………………………………………………………………………………………45
4.3. 3 Смачивание и несмачивание………………………………………………….47
4.4. Капиллярные явления………………………………………………………………49
Литература…………………………………………………………………………………………51
ПОВЕРХНОСТНАЯ ЭНЕРГИЯ
ПОВЕРХНОСТНАЯ ЭНЕРГИЯ
Избыток энергии поверхностного слоя на границе раздела фаз (по сравнению с энергией в-ва внутри тела), обусловленной различием межмолекулярных взаимодействий в обеих фазах. При увеличении поверхности раздела, т. е. при переводе молекул (атомов) в поверхностный слой, совершается против нескомпенсированных сил межмолекулярного вз-ствия у границы раздела, равная удельной с в о б о д н о й П. э. s (для жидких поверхностей она тождественна поверхностному натяжению). Полная П. э. u=s-Т(дs/дТ), где второй член представляет собой скрытую теплоту образования единицы площади поверхности (с в я з а н н а я э н е р г и я) в необратимом изотермич. процессе при тем-пре Т. Величина дs/дТ - удельная п о в е р х н о с т н а я э н т р о п и я (обычно отрицат. величина). Свободная П. э. линейно уменьшается с ростом Т, полная П. э. явл. температурным инвариантом, но для полярных жидкостей она может несколько возрастать за счёт диссоциации. Вблизи критической температуры Tкр различие св-в соседствующих объёмных фаз нивелируется и при Т= Tкр исчезает.
Физический энциклопедический словарь. - М.: Советская энциклопедия . . 1983 .
ПОВЕРХНОСТНАЯ ЭНЕРГИЯ - избыток(по сравнению с объёмными фазами) энергии поверхностного слоя между соприкасающимисяфазами, приходящийся на единицу площади разделяющей поверхности. Если последняяделит двухфазную систему А - В на части с объёмами V А и V B , то П. э. равна где U - внутр. системы, и А, плотностиэнергии в объёме фаз А и В. Аналогично определяются поверхностнаяэнтропия свободная П. э.и др. термодинамич. потенциалы. Их численные значения зависятот положения разделяющей поверхности, к-рое для плоских поверхностей обычновыбирается из условия равенства нулю адсорбции одного из компонентов (эквимолекулярнаяповерхность). В однокомпонентной системе уд. П. э.и уд. свободная П. э. (см. Поверхностное натяжение )связаны ур-нием Гиббса - Гельмгольца:
![]()
Для границы - газ ![]() - уд. энтропия) и В отличие от поверхностного натяжения П. э. слабо зависит от темп-ры.
- уд. энтропия) и В отличие от поверхностного натяжения П. э. слабо зависит от темп-ры.
Свободная П. э. определяет работу образованиязародышей новой фазы и свободную энергию акттвации процесса фазового превращения. метастабильных состояний (состояний переохлаждения, процессы диспергпрования, адгезиии смачивания. При низком значении свободной П. э. возникает самопроизвольноедиспергпрованпе фаз, происходящее, напр., вблизи критич. . Присмачивании погружением изменение свободной П. э. определяет работу смачивания(правило Дюпре). При неполном смачивании свободная П. э., входя в ур-ниеЮнга, определяет равновесную форму капли или пузыря и величину краевогоугла (см. Смачивание).
Равновесная форма анизотропного тела вобщем случае определяется минимумом свободной П. э. при заданном объёметела V
(принцип Гиббса - Кюри):
![]() V =
const (суммирование по всем возможным i
поверхностямс площадями А i
). Согласно правилу Вульфа (1895), вытекающемуиз принципа Гиббса - Кюри, равновесная форма монокристалла характеризуетсяналичием точки (точки Вульфа), расстояния h i
от к-ройдо граней кристалла пропорциональны их свободным П. э.:= const. Чем выше свободная П. э. грани, тем меньше её вклад в свободнуюП. э. всего кристалла. В соответствии с принципом Гиббса - Кюри для изотропноготела равновесная форма - шарообразная, она присуща каплям и пузырям в отсутствиевнеш. полей. Этот принцип определяет также форму мицелл (см. Поверхностно-активныевещества, Полимеры).
V =
const (суммирование по всем возможным i
поверхностямс площадями А i
). Согласно правилу Вульфа (1895), вытекающемуиз принципа Гиббса - Кюри, равновесная форма монокристалла характеризуетсяналичием точки (точки Вульфа), расстояния h i
от к-ройдо граней кристалла пропорциональны их свободным П. э.:= const. Чем выше свободная П. э. грани, тем меньше её вклад в свободнуюП. э. всего кристалла. В соответствии с принципом Гиббса - Кюри для изотропноготела равновесная форма - шарообразная, она присуща каплям и пузырям в отсутствиевнеш. полей. Этот принцип определяет также форму мицелл (см. Поверхностно-активныевещества, Полимеры).
Кроме П. э. и её аналогов в термодинамикеповерхностных явлений рассматриваются характеристики межфазных линий, к-рыемогут возникать как при пересечении поверхностей, так и в пределах однойповерхности, если на ней происходит двумерный . Избытокэнергии на межфазной линии называют линейной энергией. Существуют понятиялинейной свободной энергии и др. одномерных аналогов поверхностных величин. краевой угол малых капель ипузырьков на жидкой и твёрдой поверхности. Линейная вноситвклад в формирование равновесной формы малых кристаллов.
Лит.: Русанов А. И., Фазовые равновесияи , Л., 19С7; Гиббс Д. В., Термодинамика. Статистическаямеханика, пер. с англ., М., 1982; Роулинсон Дж., Уидом Б., Молекулярнаятеория капиллярности, пер. с англ., М., 1986.
А. И. Русанов.
Физическая энциклопедия. В 5-ти томах. - М.: Советская энциклопедия . Главный редактор А. М. Прохоров . 1988 .
Смотреть что такое "ПОВЕРХНОСТНАЯ ЭНЕРГИЯ" в других словарях:
Энергия, сосредоточенная на границе раздела фаз, избыточная по сравнению с энергией в объеме. При увеличении пов сти раздела фаз уд. полная П. э. (на единицу пов сти) e характеризует увеличение энергии системы. Она равна сумме мех. работы s… … Химическая энциклопедия
Избыток потенциальной энергии вещества, определяемой всеми взаимодействиями частиц, у поверхности какого либо тела по сравнению с энергией в объеме … Большой Энциклопедический словарь
Избыток потенциальной энергии вещества, определяемой всеми взаимодействиями частиц, у поверхности какого либо тела по сравнению с энергией в объёме. * * * ПОВЕРХНОСТНАЯ ЭНЕРГИЯ ПОВЕРХНОСТНАЯ ЭНЕРГИЯ, избыток потенциальной энергии вещества,… … Энциклопедический словарь
поверхностная энергия - paviršinė energija statusas T sritis Standartizacija ir metrologija apibrėžtis Paviršinio sluoksnio dalelių energijos perteklius palyginti su jų energija fazės tūryje. atitikmenys: angl. surface energy vok. Oberflächenenergie, f rus.… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
поверхностная энергия - paviršinė energija statusas T sritis chemija apibrėžtis Paviršinio sluoksnio dalelių energijos perteklius, lyginant su jų energija fazės tūryje. atitikmenys: angl. surface energy rus. поверхностная энергия … Chemijos terminų aiškinamasis žodynas
поверхностная энергия - paviršinė energija statusas T sritis fizika atitikmenys: angl. surface energy vok. Oberflächenenergie, f rus. поверхностная энергия, f pranc. énergie superficielle, f … Fizikos terminų žodynas
В термодинамике, избыток энергии в тонком слое вещества у поверхности соприкосновения тел (фаз) по сравнению с энергией вещества внутри тела. Полная П. э. складывается из работы образования поверхности, т. е. работы, необходимой для… … Большая советская энциклопедия
Избыток энергии поверхностного слоя на границе раздела фаз по сравнению с соответствующей объёмной энергией самих фаз, обусловленный различием межмолекулярных взаимодействий в обеих фазах. П. э. пропорциональна площади поверхности раздела фаз,… … Большой энциклопедический политехнический словарь
Избыток потенциальной энергии в ва, определяемой всеми взаимодействиями частиц, у поверхности к. л. тела по сравнению с энергией в объёме … Естествознание. Энциклопедический словарь
ПОВЕРХНОСТНАЯ ЭНЕРГИЯ - – избыток энергии поверхностного слоя на границе раздела фаз, обусловленный различием межмолекулярных взаимодействий в обеих фазах … Палеомагнитология, петромагнитология и геология. Словарь-справочник.